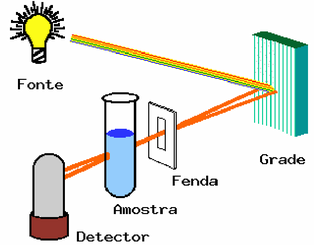
Absorção da radiação Ultravioleta e visível
Alguns espectros da região visível 1,2,4,5-tetrazina que foram obtidos sob diferentes condições: em fase gasosa (a), em fase liquida (b), e em solução aquosa (c). Observe que na fase gasosa as moléculas individuais de tetrazina são suficientemente separadas umas das outras para vibrar e girar livremente, portanto, muitos picos de absorção individuais que resultam de transições entre vários estados vibracionais e rotacionais aparecem no espectro. No estado líquido e em solução, contudo as moléculas de tetrazina não conseguem girar livremente, assim não vemos uma estrutura fina no espectro. Além disso as colisões frequentes e as interações entre a tetrazina e as moléculas de água causam uma modificação energética irregular nos níveis vibracionais e geram um espectro com o formato de uma banda única e larga.
Postado por: Lucieli Raymundi
Fonte: Fundamentos de química analítica, Skoog;